开发一种新型吸入治疗用于治疗支气管炎梗阻栓塞综合征
虽然肺移植已成为末期肺病的成熟治疗选择,但不幸的是延长的受助人的生存仍然是一个挑战。在移植后的长期存活的主要因素是支气管炎梗阻症综合征(BOS),否则被称为灭错的支气管炎(OB),毁灭性和致命的疾病。博斯是肺移植后死亡的主要原因,近50%的患者在移植后五年内开发博斯。
了解闭塞性细支气管炎综合征
闭塞性细支气管炎综合征是一种阻塞性气道疾病,引起细支气管壁的炎症和纤维化,并使细支气管直径减小。该病可迅速发展,通常在确诊后一至两年内出现呼吸衰竭和死亡。BOS常见于肺移植和异基因造血干细胞移植(alloHSCT)后的患者,尽管它也与自身免疫性疾病和环境污染物暴露有关。根据公司的市场研究,在美国、欧洲和日本,估计有21500名肺移植患者和8500名异器官移植患者目前受到BOS的影响。

除了对BOS患者的身体后果和对BOS患者及其照顾者的心理健康的潜在负面影响外,这种疾病还带来了经济负担。美国医疗保健利用数据显示,与无肺移植患者相比,使用BOS治疗肺移植患者的成本每年增加30- 40%。尽管存在重大的人文和经济负担,但目前还没有批准的BOS治疗方法。
推进式吸入呼吸疗法
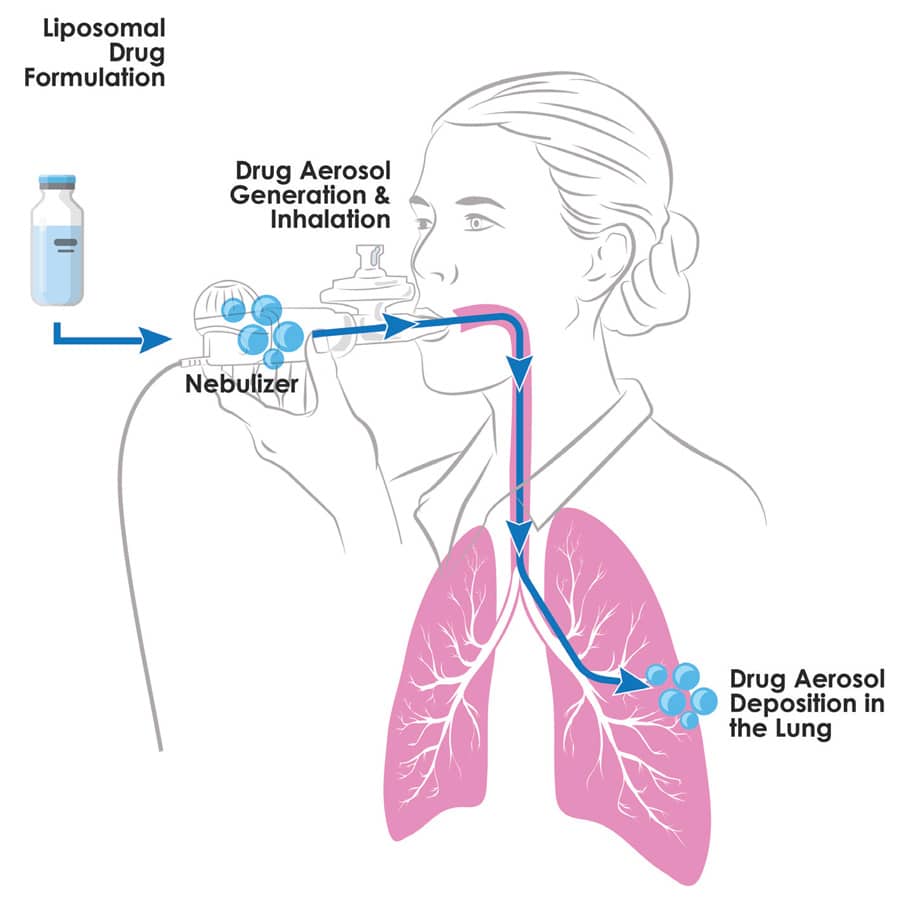
Breath Therapeutics成立于2016年,于2019年7月被Zambon S.p.A.收购,由首席执行官Jens Stegemann博士领导,Breath团队由在药物配方和制造、气雾剂给药、临床开发和商业化方面具有专业知识的多技能专业人员组成。这家总部位于美国和欧盟的公司开发了环孢素a的一种新型脂质体制剂,称为L-CsA-i,通过PARI制药公司开发的试验性eFlow®喷雾器系统直接应用于肺小气道。eFlow®喷雾器系统是专门为L-CsA-i设计的,允许药物输送到肺部的靶区。它是专为家庭吸入额外方便患者。

L-CSA-I目前处于实验阶段,并已从美国食品和药物管理局和欧洲药物局接受孤儿药物的孤立,以治疗BOS。在撰写本文时,临床试验中有1,100个患者L-CSA-I暴露。L-CSA-I是一种调查药物,尚未建立其安全性和疗效。
博斯可以在呼吸衰竭和诊断后一到两年内发生呼吸衰竭和死亡。
吸入交付的理由
全身施用的环孢菌素A(CSA)通常使用肺移植和AllOHSCT以防止急性肺同种异体移植排斥或急性和慢性接枝与宿主疾病。在通常的目标系统浓度下的系统施用模式中,CSA不能在支气管中的疾病部位达到足够的药物水平以治疗BOS。吸入疗法的潜在优势是将药物直接递送到疾病的部位并降低全身暴露。
L-CSA-I临床试验,用于治疗BOS
该公司正在进行五项临床试验,评估L-CSA-I的安全性和功效。波士顿发展计划旨在评估L-CSA-I的使用,以治疗六岁及以上患者的植物。波士顿计划在现有研究中建立,表明局部监禁在航空中的免疫抑制剂可能是治疗博斯的潜在选择。
波士顿-1和波士顿-2临床试验于2019年3月开始。波士顿-1正在评估L-CSA-I,用于治疗BOS
呼吸治疗性的使命 - Zambon集团公司是将第一个安全有效的待遇与BOS的人民一起。
在单肺移植接受者中,Boston-2将相同的方法与BOS一起使用与双肺移植受者一起使用。两项试验将在八个国家的35个主要肺部移植专业中心注册共同参加220名参与者。在完成48周的试验后,参与者将有资格在波士顿-3继续,这是波士顿-1和波士顿-2的开放标签扩展试验。

计划两项额外的临床试验。Boston-4的目标参与者是AllOhsct的成人受体。波士顿5将在6至17岁的儿科患者中研究L-CSA-I。
呼吸治疗方法 - Zambon Group公司致力于为BOS的人开发潜在的第一疗法。

个人反应
您的候选人的短期和长期目标是什么?
与此同时,商业团队正准备在收到美国,欧洲和其他地区的必要监管批准后向博斯带来L-CSA-I。我们的终极使命是为博斯的人提供第一个安全有效的待遇,这是一个具有紧急未满足的医疗需求的服务不足的社区。

