合成细胞也有感觉
生物学家和哲学家长期以来一直在思考这个问题,“生命的标志是什么?”当许多科学家试图以我们周围看到的生物体为基础,采用自上而下的方法来解决这个问题时,刘教授和诺瓦罗教授则是另一种自下而上方法的先驱。他们的长期目标是从零开始构建一个有功能的活细胞,这是以前从未做过的事情,但通过他们的努力,现在看来是可以实现的。
最低限度的生命
为了制造合成细胞,Liu和Noireaux确定了三个他们认为定义功能性活细胞的基本“模块”。他们的目标是将这些模块放在实验室中,首先构建能够再现复杂生物功能的“最小细胞”模型。这是迈向完整的最小细胞(只显示生命的最低要求的细胞)之前的必要步骤,并在此过程中,表征了维持生命所需的基本元素。
这三个基本模块是信息(构建细胞组件的指令,保存在DNA序列中)、代谢(能量生成、构建模块的合成和循环)和自组织(在物理边界内封装信息和代谢)。这三个项目都包括在Liu和Noireaux的国家科学基金会(NSF)项目中,“构建具有膜机械敏感功能的DNA程序化最小细胞”。
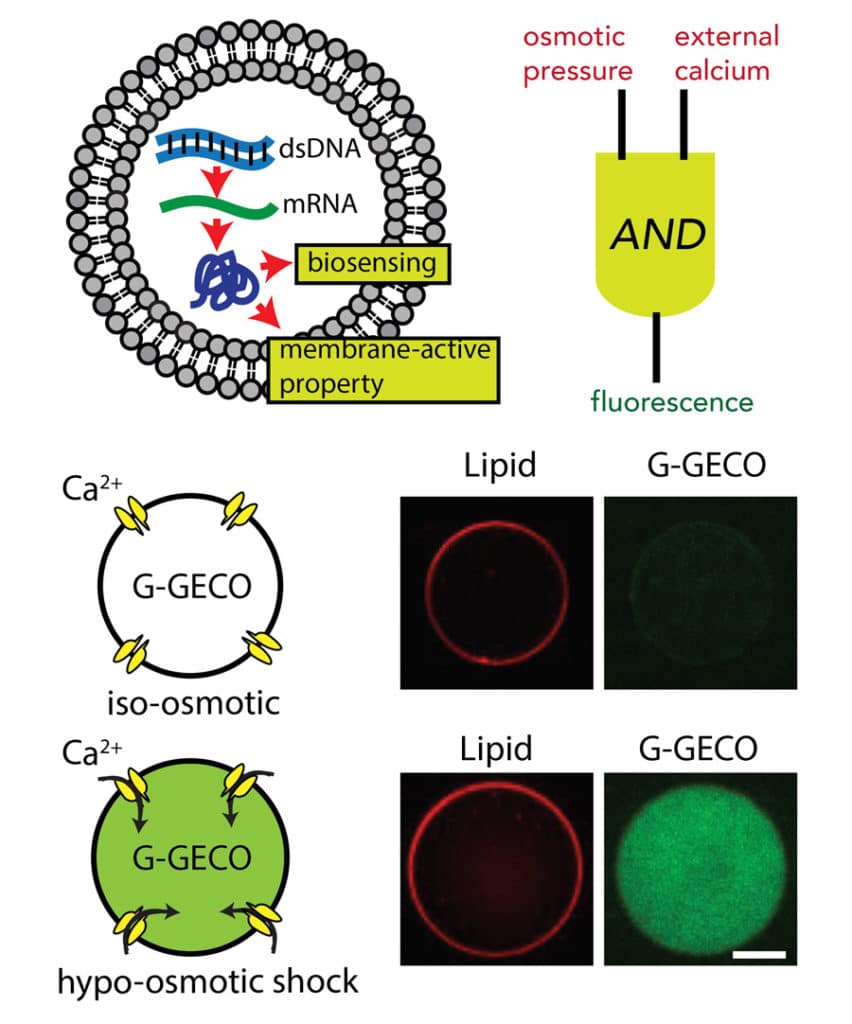
图改编自Majumder, Garamella等人,化学通讯, 52,7349 -7352, 2017。
虽然合成生物细胞的构建现在看来是可行的,但还没有从基本分子中构建出具有功能的最小细胞。Liu和Noireaux认为,他们的模块化方法应该能够通过精心设计的连接将多个分子组件整合起来,从而创造出能够整合多种细胞功能的人工细胞。
信息就是力量
利用大肠杆菌分子机制的原理,Liu和Noireaux开发了一种无细胞系统,可以将DNA序列中的信息转录和翻译成执行细胞功能的蛋白质。转录(将DNA代码复制到一个RNA模板分子上)和翻译(使用这个RNA模板构建蛋白质)都是在该团队独特的无细胞转录-翻译(TXTL)系统中完成的,这个系统构成了他们最小细胞的基础。TXTL系统已经被工业用作合成蛋白质的替代方法,但它在实验室中的作用更令人兴奋。
组织是关键
在密歇根-明尼苏达系统中,TXTL机制被包裹在一个叫做脂质体的细胞大小的小隔间里。脂质体利用了脂肪不溶于水这一简单事实。双分子层,每个包括亲水(亲水)集团如磷酸盐和疏水性(脂)组件,在水中的时候,会自发形成一个包围的球体,定位与脂质指向中心的膜,保护从水中磷酸基的两侧。这些磷脂双层膜在本质上直接类似于围绕细胞的细胞膜。一旦TXTL系统被封装到脂质体中,这个系统就能满足生命所需的前两个模块:在受控的环境中,使基因程序得以执行,以刺激细胞的构建和功能。
磷脂双分子层是自然界中环绕细胞的膜的直接类似物
使新陈代谢
在将信息系统包裹在脂质体内之后,构建最小细胞的最后,或许也是最具挑战性的部分是使其能够与外界进行沟通。为了新陈代谢、生长和繁殖,最小的细胞必须能够通过它的膜吸收能量,从相反的方向排出废物,并对从周围环境接收到的信号作出反应。
Liu和Noireaux目前的工作重点是整合脂质体膜上的分子通道,这些通道通过打开或关闭对环境刺激作出反应。他们以大肠杆菌中发现的另一种系统为模型,构建了一个编码名为MscL的膜通道蛋白的DNA序列。MscL是“机械敏感”的,也就是说,它会根据渗透压(渗透压是由周围水和脂质体内部溶解分子的浓度差异造成的压力)的变化而开启和关闭。
为了测试MscL通道的功能,他们还在最小细胞的DNA中编码了一种名为G-GECO的工程蛋白,这种蛋白会对钙离子产生荧光反应。因此,当仅存在于外部的钙分子通过MscL穿过细胞膜时,G-GECO通过荧光反应。
生物的“与门”
Liu和Noireaux将这个最小的细胞系统描述为合成的、生物敏感的“与门”(一个需要两个输入来产生反应的系统)。在这种情况下,两个输入是机械(渗透压)和化学(钙离子)。当渗透压使MscL通道打开时,钙离子流过脂质体并激活G-GECO。因此,这对夫妇说,“我们已经生成了一个dna编程的细胞大小的人工细胞,它可以感知渗透压和外部钙离子浓度。”
他们现在的目标是将这种激活与脂质双分子层的物理生长(从而使细胞成为一个整体)结合起来,将其与遗传控制的由较小前体分子合成的脂质结合起来。通过这种方式,机械敏感膜将促进细胞结构与其DNA之间的关键联系,这是迈向真正合成生命的关键一步。
这项研究为创造能够感知和响应环境的最小细胞铺平了道路
比生物学?
Liu和Noireaux的研究为创造能够感知和响应环境的最小细胞铺平了道路,这是合成生物学迄今为止一直难以实现的关键一步。他们的系统提供了一个实验平台,能够快速和可靠地量化操纵最小细胞系统的任何方面的效果:膜,周围的溶液和遗传机制。这应该会加快微小细胞工程的未来进展,最终可能会扩展在自然生物细胞中发现的特性。
这个项目在很大程度上依赖于实验室、机构和学科之间的合作,以解决诺瓦罗所称的合成最小细胞的“具有挑战性但可以想象的目标”。位于生物学和工程学交界处的这项研究增加了我们对生命的基本知识,促进了医学(如药物输送)和生物技术的进步,并为未来在这些机构进行研究的科学家提供了一个基于基本生物和物理原理的前沿研究的令人兴奋的介绍。Noireaux说,这不是“仅仅是一种练习”,而是一种“前沿工程方法”。
常见问题
是什么让你开始研究“最小细胞”这个概念?
TXTL系统与以前建立最小细胞的方法有何不同?
为什么膜通道的合并如此重要?
下一步你想在你的最小细胞中加入什么基因或功能?
你认为这项研究在十年后会走向何方?