一种提高癌症免疫疗法的新武器
在过去的几年里,免疫疗法已成为癌症治疗的主要方法之一。免疫疗法刺激免疫系统更有效地破坏肿瘤,可用于单疗法以及与其他癌症治疗或手术组合使用。现在,科学家通过增强肿瘤细胞免疫原性,增加肿瘤部位的免疫细胞数或通过阻断癌细胞产生的特定分子来抑制免疫系统对肿瘤的攻击的特定分子来进行切除免疫疗法的方法。
由Svetlana Hamm博士领导的4SC研究和转化医学小组发现了一种特别令人兴奋的免疫治疗组合方法。她和她的团队正在探索一种名为domatinostat的HDAC(组蛋白去乙酰化酶)抑制剂的潜力。dominostat与免疫疗法协同工作,特别是针对PD-1/PD-L1(程序性死亡蛋白1和pd -配体1)轴的免疫疗法,目的是重新启动免疫系统对肿瘤的攻击。
癌症免疫和PD-1 / PD-L1轴
细胞中的遗传突变可导致细胞过程的失调和不受控制的细胞增殖,最终导致肿瘤内血。另一方面,突变和失调的基因表达导致肿瘤细胞产生肿瘤抗原和释放信号,将它们标记为外国和对生物危害。根据该过程对身体的看法有何看法,免疫系统将响应和消除此类细胞。然而,通常癌细胞仍然被忽视或设法阻止免疫发作。
Domatinostat旨在重新启动免疫系统对肿瘤的攻击,并与靶向PD-1 / PD-L1轴的免疫疗法一起工作。
免疫反应通常包括免疫系统的特定细胞,即所谓的细胞毒性T细胞(CTLs),涌入肿瘤部位。这些细胞通过识别肿瘤抗原特异性地杀死肿瘤细胞。然而,肿瘤细胞可以通过上调表面的PD-L1分子来阻止这种攻击。PD-L1与ctl上表达的抑制性PD-1受体结合,阻断它们的活性,使它们基本上失去作用。所谓的检查点封锁是一种免疫疗法,它阻止PD-L1分子与CTL的PD-1受体结合,从而释放CTL攻击肿瘤细胞。尽管这种方法在许多病例中取得了成功,但患者的反应在不同癌症类型和患者个体之间存在很大差异。这可能是由于缺乏肿瘤特异性免疫反应,肿瘤特异性抗原递呈下调,或癌细胞产生的免疫抑制细胞和分子抑制CTL功能,而不依赖PD-L1的作用。
癌细胞有许多防御机制
肿瘤可以显示不同水平的免疫系统受累。“热”肿瘤具有肿瘤免疫微环境中存在的CTL,但正在积极表达PD-L1作为抑制CTL攻击的防御(见图1,面板2,3和4).“冷”肿瘤在其微环境中没有免疫细胞,很可能已经避免了免疫检测,所以这些肿瘤细胞不需要上调PD-L1面板(1).在这种情况下,治疗的目的是“加热”肿瘤并导致CTL渗透。然后通过阻断PD-1 / Pd-L1相互作用,检查点抑制剂可以有助于肿瘤特异性免疫应答,导致杀伤癌细胞面板(2).
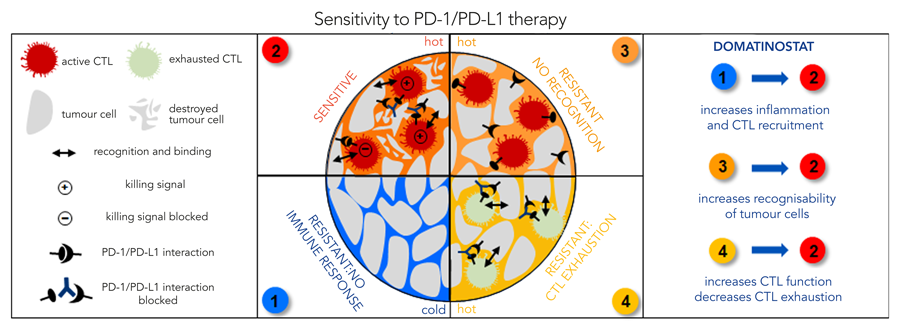
不幸的是,肿瘤会反击。肿瘤细胞试图通过下调抗原呈递来避免被ctl识别和结合面板(3),或它们募集免疫抑制细胞,其抑制CTL功能。结果,即使在PD-1 / PD-L1被成功阻断的情况下,微环境仍然是为了抑制CTL的有效性。然后将CTLS处于所谓的耗尽状态,从而无效(面板4).因此,需要一种可以与检查点治疗一起工作并补充的药物。
HDAC抑制剂是一组已显示的合成分子,这些分子以增加癌症抗原的表达及其对CTL的表达,以及通过产生吸引免疫细胞的细胞信号在肿瘤中产生肿瘤微环境中的CTL的数量。
作为特定HDAC抑制剂的Domatinostat先前已经过测试并显示出有前途的抗癌活性作为单一疗法。鉴于PD-1 / PD-L1封闭的有效性依赖于微环境,哈姆和她的团队在4SC中提出了Domatinostat的增加会打击导致检查点治疗的抗性。


在携带肿瘤的小鼠中测试dominostat
第一步是在带有不同类型CTL水平肿瘤(“热”或“冷”肿瘤)的老鼠身上测试dominostat。然后用domatinostat和PD-1/PD-L1阻滞剂(已建立的人类检查点抑制剂的小鼠特异性类似物,如nivolumab、pembrolizumab或avelumab)治疗小鼠。CT26肿瘤被认为是一种非炎症(冷)肿瘤,而C38肿瘤被认为是炎症(热)肿瘤。
结果很清楚。在冷CT26肿瘤中,单独的Domatinostat将肿瘤大小降低一半并增加CTL的数量八倍(见图2).此外,治疗触发了免疫相关的细胞机制,增强了炎症,并将肿瘤变成了热点肿瘤。Domatinostat还通过上调肿瘤抗原的产生和它们在细胞表面的呈现,增加了肿瘤细胞对ctl的识别性。当联合使用dominostat和PD-1/PD-L1阻断剂时,抗肿瘤作用进一步增强,而单独使用PD-1/PD-L1阻断剂无效。
Domatinostat始终改善肿瘤免疫微环境的组合物,以最大限度地提高成功PD-1 / PD-L1封闭处理的可能性。
热C38肿瘤模型的结果同样令人印象深刻。虽然C38肿瘤已经容纳了大量的ctl,但这些细胞无法消除肿瘤,因为它们处于衰竭状态。因此,单独阻断PD-1/PD-L1在这种类型的癌症中只有很小的影响。然而,Domatinostat使这些肿瘤中的ctl数量增加了近两倍,更重要的是,还增加了它们的活性和有效性。因此,无论是单独使用dominostat还是与PD-1/PD-L1阻断剂联合使用,都大大延长了生存时间,使50%以上的实验动物完全愈合。
加入鸡尾酒
MHC-II(主要组织相容性复合物-II)是存在于细胞表面上的蛋白质。它们支持产生额外的肿瘤特异性CTL类型,从而提高肿瘤的免疫发作。已显示Domatinostat以增加肿瘤中的MHC-II分子。然而,对免疫反应产生的这种有益效果通常被发现由于MHC-II与另一抑制CTL受体LAG3的结合而对CTL活性的负面影响,这与PD-1类似地阻断CTL的功能.因此,在携带肿瘤小鼠的另一个实验中,哈姆博士和她的团队在4SC中加入了Domatinostat和PD-1 / PD-L1封闭的混合物。这导致甚至更高的抗肿瘤活性,肿瘤在80%的动物中回归。

在这种情况下,另一个重要的成分是一种叫做4-1BB的细胞分子,它是ctl的共刺激受体。共刺激是ctl充分发挥作用所必需的一种机制。4-1BB鼓励CTL增殖,当CTL耗尽时,像4-1BB这样的共刺激受体可以部分恢复它们的细胞杀伤能力。事实上,4-1BB的联合刺激被发现比PD-1/PD-L1阻断更有效,在这些难以治疗T细胞枯竭的肿瘤中,应答率为35%。值得注意的是,当添加dominostat时,应答率翻倍至70%。
敏感试验
下一步是测试人类患者的Domatinostat。敏感试验是一个正在进行的临床试验,观察与单独的黑色素瘤的患者单独响应检查站封锁 - Domatinostat的理想设置(Hassel等,2019)。
在该试验中,Domatinostat在添加检查点封闭之前将作为单药治疗给予单药治疗。4SC团队监测在Domatinostat施用前后患者的肿瘤中相关基因的表达。他们观察到癌症抗原的表达增加,抗原呈现和增强的第一个评价患者中的炎症,其证实了从前的动物试验中的观察结果,并意味着对随后用检查点抑制剂治疗的敏感性增加。
从工作台到床边
dominostat在这些早期试验中证明了自己是PD-1/PD-L1抑制剂的非常有效的联合伙伴。如上所述,它不仅通过增加肿瘤微环境中CTL的数量,还通过增强CTL的活性和有效性,以及激活对抗癌细胞抗性机制的免疫途径来实现这一目标。这些效果预计将特别适用于癌症,如黑色素瘤、默克尔细胞癌(MCC)、尿路上皮癌和大肠癌。
这些早期的生物标志物从敏感试验中获得Domatinostat治疗非常令人鼓舞,整个4SC团队期待继续开发这种潜在的练习改变药物的组合免疫疗法。
个人反应
到目前为止,在接受测试的患者中毒性表现如何?

