目标蛋白质降解:疾病治疗的新方向
蛋白质是大型且复杂的分子,具有几乎不想到的广泛的角色和功能。在人体内,蛋白质充当积木,使者和运输车。作为酶,蛋白质有助于向我们的细胞提供能量并读取我们的DNA。作为抗体,他们捍卫我们的疾病。蛋白质也在疾病中发挥关键作用。例如,当我们的身体感染细菌时,它是造成伤害的细菌蛋白质。当读取或修复我们的DNA的蛋白质出错时,癌细胞可以形成。
阻断致病蛋白的功能是目前许多药物治疗的一个重要目的。虽然这在一开始是有效的,但随着时间的推移,限制可能会出现。大剂量和/或持续的治疗可能导致毒性副作用或对药物的耐受性。在最糟糕的情况下,可能会出现对治疗的完全耐药性。

为了克服这些问题,所有部门的研究人员都在研究一种新的策略,称为靶向蛋白质降解。他们并没有把重点放在阻止有害蛋白质功能的药物上,而是在寻找摧毁这些蛋白质的方法。这可以通过两种被称为PROTACs(蛋白水解靶向嵌合体)和分子胶的药物来实现。这些药物能将有害蛋白质从细胞中清除。为了帮助这些努力,丹尼尔斯、里奇和乌尔博士正在积极开发新技术,以描述和研究这些化合物在细胞内的功能,从而更快地对早期化合物进行分类,以发现有效的化合物。
一个潜在的解决方案
细胞已经有一个非常聪明的、固有的垃圾处理系统,用于正常的、有调节的蛋白质破坏。像protac这样的药物只是将有害蛋白质带入或传送到这个系统。然后,细胞自身的机制完成剩下的工作——分解或降解蛋白质,使它们不再造成伤害。
研究表明,与其他类型的药物相比,protac在低剂量下具有更有效和更持久的潜力。
这种细胞垃圾处理系统被称为泛素-蛋白酶体途径。PROTACs能够收集有害蛋白质并将其摧毁。像任何药物一样,PROTACs必须先穿过细胞膜进入细胞。下一步,被称为三元络合物形成,是PROTAC发挥其魔力的地方。在这一步骤中,PROTAC或分子胶将目标蛋白连接到关键的蛋白降解机械复合物。这个复合物的形成是一个关键步骤,因为它允许蛋白质被标记为随后的降解。这是通过一种叫做泛素化的过程发生的,在这个过程中,一种叫做泛素的小蛋白质的多个副本被添加到目标致病蛋白质中。
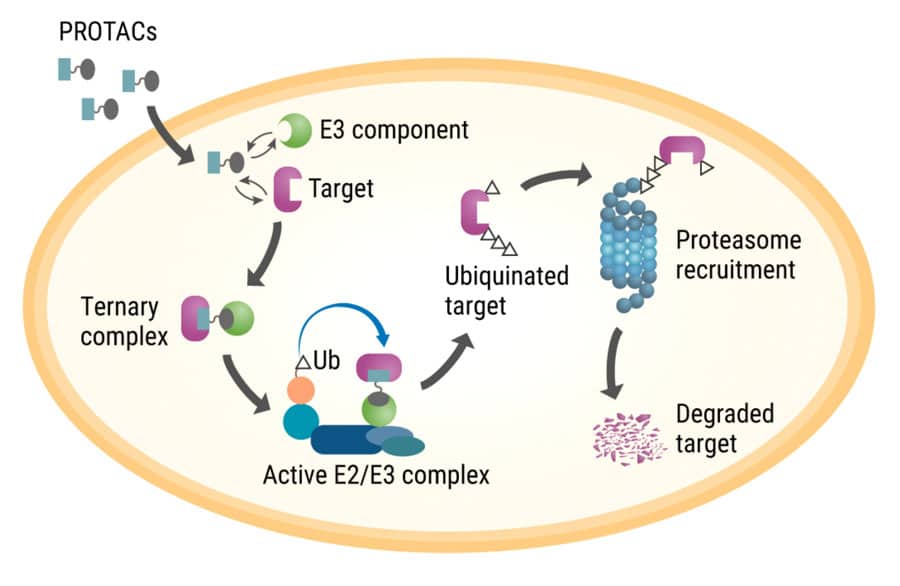
一旦通过泛素定量标记靶蛋白,就像接受死亡的吻一样,然后将蛋白质运输到称为蛋白酶体的大分子结构(您可以将其视为细胞的再循环中心)。该蛋白酶物体将靶蛋白分解为其组分份,细胞可以用于各种功能,包括作为新蛋白质的构建块。
一些研究表明,单个PROTAC药物分子可以重复使用,多次重复蛋白质破坏循环,降解有害蛋白质的多个副本。这就解释了为什么最初的研究表明,与其他类型的药物相比,protac在低剂量下具有更有效和更持久的潜力。
描述PROTACs
显然,PROTACs作为一种新的治疗方式具有巨大的潜力。然而,有一个问题是,由于获得成功所需的过程非常复杂,很难评估PROTACs在细胞内如何以及在何处工作。用于评估药物在细胞内功能的传统方法不适用于PROTACs。例如,像western blotting这样测量靶蛋白水平的方法很难用于对数千种不同药物化合物的高通量筛选。此外,蛋白质降解是一个动态过程,因此需要在多个点上检查蛋白质水平,以了解随着时间推移的降解过程。

Promega团队正在利用CRISPR/Cas9技术和添加发光蛋白标签的基因组编辑技术开发新方法,直接解决这一筛选问题。这种多管齐下的方法使内源性靶蛋白(有望被PROTAC降解)的数量在药物起作用的时间段里容易被跟踪和测量。越来越受欢迎的CRISPR/Cas9技术来自细菌中自然发生的基因编辑系统,对这些研究至关重要。它允许DNA在特定的点被切割,然后DNA可以被添加、删除或改变。
在PROTACs的研究中,CRISPR/Cas9已经被用来用一种名为HiBiT的标签来标记目标蛋白质,当这种标签与它的伴侣结合时,会在活细胞中产生明亮的发光,类似于萤火虫在夜空中发光的方式。在这种情况下,测量PROTAC处理后的细胞的发光情况,就可以表明有多少致病蛋白质存在,因此药物的效果如何;荧光信号越低,靶蛋白含量越低,药物疗效越好。最重要的是,这项技术允许实时跟踪致病蛋白质——研究人员可以实际观察到经protac处理的活细胞中的蛋白质降解。
研究人员实际上可以观察到在protac处理过的活细胞中蛋白质的降解。
深入蛋白质降解
利用CRISPR/Cas9技术结合发光技术实时跟踪蛋白质降解是一个巨大的进步。然而,研究小组希望通过调查蛋白质降解过程中的每个关键步骤,进一步深入蛋白质降解系统。如果细胞要开始它的垃圾处理程序,三元配合物的形成是必要的。即使PROTAC的化学成分发生了非常小的变化,也会影响复合物的形成:使其稳定或不稳定,或完全阻止其形成。了解三元配合物是如何形成的,以及它们能维持多久,将有助于改进PROTAC的设计。三元配合物可以通过生物发光能量转移(BRET)检测,只有当两个蛋白质靠近时才会发生,这表明蛋白质在一个配合物中。

BRD4 protac ARV-711将在各种浓度上添加到CRISPR Hibit-BRD4细胞中,并且在Glomax发现微孔板读卡器上每5-15分钟连续监测活细胞发光。当HIBIT-BRD4蛋白降解时,观察到发光丧失。ARV-711 Protac损失的蛋白质的速率和程度高度依赖于所使用的药物浓度。降解图可用于对化合物的排序效力和疗效进行排序。
然而,可能比三元络合物形成更重要的是泛素化。这不仅需要三元配合物的形成,还需要目标蛋白位于包含三元配合物的更大的活性配合物的正确位置。然后,泛素就可以转移到靶标上。泛素化的量是很重要的:它必须超过一定的水平,目标蛋白才能被标记以进行降解。同样,当目标蛋白和泛素在一起时,可以使用BRET检测活细胞中的泛素化水平。
更深入地了解降解途径中的每一步,可能会使PROTACs在每个阶段的作用得到优化。这将有助于研究人员开发出最有效、最精确的PROTAC疗法,以治疗传统药物难以治疗的疾病。
未来的药物?
Protacs的发展仍处于早期阶段。然而,像Promega团队这样的研究人员认为这类药物的发展将在未来几年继续迅速增加。对于Protacs来实现他们的潜力 - 并且最终,对于患者来利益 - 需要对这些药物的行动进行彻底评估这些药物。对于任何给定的目标,存在许多可能的protacs变化,并且每个必须对其他目标进行分析并排名。确定那些值得进一步发展的人是研究人员的下一个挑战。

在不破坏细胞或干扰细胞过程的情况下,标记和测量活细胞内的有害蛋白质是PROTAC发展的重要组成部分。利用CRISPR/Cas9等技术引入发光标记,然后利用能量转移来研究蛋白质相互作用,是迈向成功的重要一步。随着对蛋白质降解途径的认识不断扩大,一种更有效、更少有害的治疗一系列严重疾病的方法开始出现。
个人反应
在PROTACs和分子胶成为标准/被接受的治疗方法之前需要做什么?

