面向量化个化肿瘤
半数以上癌症患者在护理期间某点接受辐射处理辐射理疗比任何其他肿瘤治疗都频繁开药
当前辐射协议
当前,辐射处理涉及向病人提供最大可容忍剂量协议建立多度升级测试 提高平均生存率不幸的是,病人副作用可能包括重辐射毒物辐射还被认为提升免疫系统帮助治癌研究显示,放射性治疗的成功完全可能是通过直接细胞毒性杀死肿瘤细胞的组合,也许更重要的是,它反声波免疫效果当前辐射协议不侧重于增强这些免疫响应研究显示,各种辐射剂量以不同速率刺激抗波豁免研究者通过直接辐射细胞毒性和随后反脉冲免疫反应优化合并细胞死亡

Heiko Enderling博士和Rachel Howard博士 综合数学肿瘤系H佛罗里达州LeeMoffitt癌症中心研究所与波兰科学院Jan Poleszczuk博士和德国Helmholtz中心Juan CarlosLopis Alfonso博士一起,正在整合数学、生物学和临床科学为个体病人建模、模拟预测处理响应开发各种数学模型计算最佳辐射协议和最优处理时间他们的作品位居“虚拟测试”前列,个人化癌症处理,为每位病人提供最优适应性癌症治疗
仿真癌症
研究者观察有转移式癌症的病人癌症细胞从最初形成地传播到身体的另一部分癌症细胞脱离初始肿瘤并穿透血液或淋巴系统,在别处形成新肿瘤新的代向肿瘤与原肿瘤相同类型,尽管位于别处Enderling博士及其团队研究辐射场外肿瘤响应,即Abscopal特效向量性疾病患者单肿瘤点辐照也会导致病人身体其他地方肿瘤回归Enderling博士解释道 : “这突显了转移性疾病通过病人免疫系统 和局部治疗的互连性,如放射治疗或甚至外科手术 改变处理场内免疫细胞数部分免疫细胞死亡,而另一些细胞则被刺激这些变化将系统化显示免疫系统遍及全体。”这些令人振奋的观察促使研究团队偏离“局部理疗”概念,以加深对辐射作为生物剂对整个体作用的理解。
研究者的工作显示,在转移性疾病中,人体不同部分的肿瘤以不同方式参与免疫监控最有意思的是,病人身体中不同癌症通过免疫系统互为依存正挑战我们目前对癌症转移的理解传统观念即肿瘤变换大时可能并不总是精确取而代之的是,某些肿瘤可能很大,因为它们转移使用如果肿瘤有强免疫应变分布体 全体, 部分免疫系统细胞 将改道到远程移位分治策略允许从免疫介质肿瘤控制中解脱Enderling博士及其团队需要识别最佳辐射处理目标,以诱导系统响应并杀非直接辐射目标肿瘤

Mathematical modelling approach
辐射常配有外科、化疗、目标代理物和免疫法等其他疗法许多可能的辐射剂量加各种疗法的不同组合不同时段对转移性疾病患者不同时段使得无法实验和临床测试所有可能的变换研究人员数学建模方法使用现有临床预科数据和临床研究结果模拟所有可能的处理协议变换Enderling博士及其团队使用机器学习优化理论概念帮助识别最有可能成功的处理方法这些处理方法随后可提交实验和临床验证
半数以上癌症患者在护理期间某点接受辐射处理
研究团队开发出数学模型模拟辐射响应、辐射诱发免疫激活、免疫检查站封锁法和肿瘤现场间交换活性T细胞(白细胞杀癌细胞类型)。模型不同于以往食肉动物系统理论构造
新模型先比较实验数据基于实验设置,肿瘤站点在不同空间分离位置建模,每个站点都配有视时量特征研究者在每个网站添加四种并存和交互组数数据:(1) 可行的癌症细胞,(2) 癌症细胞非免疫性死法,(3) 癌症细胞因免疫性死法和(4) 激活子细胞T数据配置程序允许研究人员估计模型参数后用这些预测那些实验环境尚未考虑的剂量响应
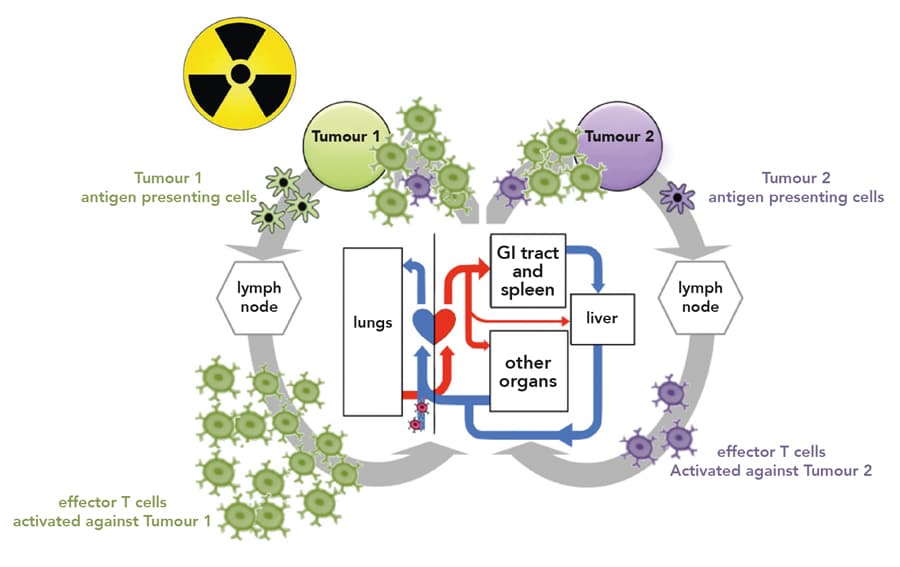
肿瘤和病人免疫系统发生复杂交互作用,其结果从消除肿瘤到肿瘤免疫并存(或休眠)和癌症细胞群快速生长不等问题变得更加复杂 当我们学习细胞毒性T细胞 遍历病人循环系统Enderling博士及其团队将局部肿瘤免疫动态和系统T细胞迁移数学模型并发,以模拟肿瘤和免疫细胞群随局部辐射演化并模拟免疫互连性其结果显示,二叉肿瘤的存在可能抑制或促进原生肿瘤生长,视其免疫增生能力及T细胞由此产生的系统再分配而定。研究者能够建模处理效果,如外科剖析和放射法估计原肿瘤量下降和整体肿瘤重负变化模型提供质相似响应临床环境报告并显示,如果转移网站通过病人免疫系统互连,则并不存在真正的局部治疗
数学肿瘤学
无数临床可行辐射量分片使得无法详尽的临床前评价综合数学肿瘤学的进展可能使这种分析成为可能。Enderling博士及其研究团队正在引入新数学模型,这些模型与实验数据相校准,以便深入破译辐射和免疫系统协同的复杂性模型估计辐射分数和辐射分量最佳分数,以获取对临床相关全效生物有效辐射分数最有利的系统免疫介质肿瘤响应允许偏离当前协议向病人提供最大可耐用剂量,一刀切方法,代之以提供病人专用精度辐射治疗并转向个性化医学
他们的作品位居“虚拟测试”前列,个人化癌症处理,为每位病人提供最优适应性癌症治疗
讨论
破土模型模拟培训具体实验数据集,以突出最有可能成功处理法重要的是,这可能有助于消除辐射目标肿瘤,以及通过激活系统免疫消除那些肿瘤和辐射场外单个癌症细胞
Enderling博士团队发现模型模拟预测显示常规辐射模式可能无法获取强效免疫介质肿瘤响应系统响应对有淋巴结参与、循环肿瘤细胞或子临床或非诊断异向沉积的向量病人特别重要,这是似然的这会为建模再增加一层复杂度,使研究人员能够平衡辐射理疗的不同生物后果,以诱导最大细胞杀戮,同时免去免疫细胞并实现随后辐射诱发豁免最大化
研究者知道,迄今为止,他们的实验数据可能偏差,而实验数据曾用于模型标定深入开发模型时,他们将使用拟议框架审查复杂转移性疾病分布,由不同器官肿瘤组合组成尽管如此,迄今为止他们的工作为评价辐射分片协议提供量化基础,以诱导免疫媒体系统反波响应持续增加合并辐射和各种免疫法的临床试验后,该模型可成为评价临床响应的宝贵工具。发人深省地说,还可以使用它帮助设计后续临床协议,并最终支持个体病人治疗规划,提供量化个化肿瘤学
个人响应
下一步向个体病人提供最优自适应癌症治疗是什么?
数学模型生成数例极感振奋的假设下一步是实验和最终临床验证数学预测生物细胞学、癌症免疫学、辐射生物学和辐射肿瘤学等实验中,我们与同事一起设计了趣味实验,以完全破译癌症复杂自适应动态,同时应对辐射理疗前后的免疫响应开始修正持续临床实验 专门收集生物标本 从生物感知器 外科和抽血样本分析肿瘤-免疫生态系统所有参与角色的作用,以及这些角色和交互作用随时间变化的方式之后,我们也许能开出辐射 不仅杀尽可能多的癌症细胞, 并意图激活强效免疫响应 帮助消除肿瘤

