病毒性脑炎和病毒介导的记忆障碍
甚至在病毒被清除后持续的持久认知缺陷是一些病毒感染的最衰弱后果之一。病毒脑炎,由进入大脑的病毒引起的,可以与慢性神经功能障碍有关,这些功能障碍可以在感染性事件中恢复后长期存在。例如,超过50%的患者患有西尼罗河病毒(WNV)的神经侵袭感染的患者体验长期认知后遗症,包括口头和探索性学习中的缺陷,可以持续数月或多年以超越急性传染性事件。
传统上认为,感染后神经功能障碍是病原体本身造成的不可逆损害。然而,在过去的几年里,越来越多的证据表明,免疫反应可能起了作用。引发的病毒感染,免疫系统的主要作用是消除病毒,但是——某种副作用——免疫细胞和分子可能会干扰神经细胞功能和沟通,负责长期的变化,防止学习,扰乱记忆,并逐步引起痴呆。
Robyn S. Klein教授和她的团队使用结合基础神经科学和免疫学(神经免疫学)、神经病毒学和神经成像方法的工具和技术来解决病毒介导的学习和记忆障碍。他们的工作重点是新出现的病毒感染,包括西尼罗河病毒(WNV)和寨卡病毒(ZIKV)。西尼罗河病毒和寨卡病毒都以神经元为靶点,并与感染后认知功能障碍有关。
在急性期
当病毒侵入大脑时,它们引发了免疫系统,其主要是目标是捍卫各种病原体的生物体。先天免疫是第一道防线。与自适应免疫(免疫系统的其他组分)不同,它不具体:无论病原体的性质如何,涉及响应感染的先天免疫防御机制。
炎症是先天免疫的主要反应之一。所有类型的脑细胞(神经元,星形胶质细胞,少曲细胞和小胶质细胞)表达免疫分子,其诱导病毒特异性细胞募集到受感染的大脑区域。目的是促进病原体清除。被细胞因子介导的(将信号从一个细胞传送到另一种细胞的小蛋白质),炎症是局部化的,并且允许脑内的感染部位被识别并清除病毒。
炎症期间出现临床症状,是急性感染的指标。实际上,免疫反应触发了行为的适应性变化,包括疲劳,疗效,减少的活动和社会互动,以及无法集中注意力。这些变化的目的是节约能源和促进生存。然而,有时,在最严重的感染病例中,炎症反应可能对神经系统缺陷,谵妄甚至昏迷进行。
虽然免疫系统在消灭病原体方面起着至关重要的作用,但免疫细胞释放的细胞因子具有多种作用,因此它们的活动可能会破坏正常的大脑功能。
慢性炎症过程
降低认知,抑郁,学习或记忆障碍是症状的例子是从急性感染恢复后可能出现的月份甚至几年。它们是大脑内传染病,慢性炎症过程的临床症状。
从历史上看,感染后神经系统后遗症已归因于由入侵病原体引起的神经元死亡或在急性期间对其的免疫应答。然而,虽然急性阶段期间的炎症是在受病毒感染的脑区域的局部化,但在急性感染中存活的患者的神经功能障碍可以影响最初感染的脑区域。因此,它可能不会直接由病毒本身引起。
神经灭绝疾病的慢性并发症实际上与持续的炎症过程有关:炎症,通过免疫反应感染急性诱导,甚至在除去病原体后仍然存在。募集免疫细胞停留在大脑中,可能影响除最初感染的细胞或地区。这导致慢性并发症,因为在免疫系统在消除病原体中起重要作用时,免疫细胞释放的细胞因子具有多种作用,因此它们的活性可能会破坏正常的脑功能。
克莱林教授和她的团队研究了持续的抗病毒免疫细胞的活动如何剥夺了内存的正常功能,以便损害学习,并且没有编码记忆。它们鉴定了调节突触塑性和神经发生的抗病毒途径的细胞因子,因此影响神经元之间的沟通,这导致感染后神经系统后遗症。
T细胞和干扰素γ
海马体是在视觉空间学习和记忆中起重要作用的大脑结构。T细胞(一种病原体特异性免疫细胞)在被西尼罗河病毒和寨卡病毒感染后恢复后仍保留在这种结构中。
Klein教授检查了从Wnv或Zikv恢复的小鼠。ZIKV主要在海马中复制,并且在恢复后,丧失神经元和后腹膜末端(神经元的部分,即在两个神经元 - 被称为突触 - 接收神经信号之间的连接水平)。WNV在整个大脑中复制,虽然没有神经元损失的迹象,但从WNV恢复的小鼠中可以看到突触终端的损失(发送神经信号的突触部分)。
虽然西尼罗河病毒和寨卡病毒对神经元有不同的影响,但两种病毒都能导致长期的认知能力下降,包括学习和记忆障碍。这表明认知后遗症依赖于一个共同的机制。
干扰素-γ (IFN-γ)是由T细胞释放的一种细胞因子,即使在感染后恢复后仍留在大脑中,它在靶向病毒方面发挥作用,但也影响突触。Klein教授报告说,缺乏IFN-γ或IFN-γ受体(因此使IFN-γ无效)的小鼠不会表现出典型的神经元或突触缺失,也不会出现任何空间学习障碍。
IFN-γ通过激活微胶质细胞(大脑中的常规巨噬细胞)介导突触消除并产生认知缺陷。实际上,在缺乏IFN-γ受体的小鼠中,感染后的小胶质细胞活化没有增加。此外,当IFN-γ受体在微胶质细胞中特异性去激活时,没有突触消除和无神经元损失,这表明小胶质细胞涉及IFN-γ介导的突触消除。
微胶质细胞和补充
补体系统由许多小蛋白质组成,它们增强免疫系统清除病原体的能力。它是先天免疫的重要组成部分。
在出生后发育早期,补体系统介导小胶质细胞的突触消除。克莱林教授表明,海马成年神经元的病毒感染诱导类似机制:在通过微胶质细胞消除突触前末端需要补体系统。实际上,具有较少的小凝血症或补体系统缺乏的小鼠免受WNV诱导的突触末端损失。
克莱林教授和她的团队研究如何
持续的抗病毒免疫细胞的活动破坏了正常的记忆功能。
因此,Klein教授团队的研究解释了病毒感染是如何引发长期认知能力下降的:感染后,留在海马体中的T细胞释放IFN-γ,激活小胶质细胞。小胶质细胞与补体系统合作,消除突触,从而导致认知功能障碍。
星形胶质细胞和白细胞介素-1
星形细胞,为神经元提供营养和承担其他角色的星形细胞,也参与了感染后神经后遗症的发展。Klein教授和她的同事证明,在西尼罗河病毒感染后,另一种由免疫细胞表达的细胞因子,白细胞介素(IL)-1,促进活化星形胶质细胞的生成。
海马体的一个特性是成年神经发生发生在那里:成年神经干细胞进化成新的神经元或星形胶质细胞。这个过程受到多种因素的调节,包括局部分子、运动、衰老和炎症。IL-1是这些因素之一,导致神经发生脱轨有利于星形发生。
IL-1是一种细胞因子,它调节一种被称为效应T细胞的抗病毒T细胞,例如,它导致发烧,这是免疫防御机制之一。它还涉及空间学习和记忆;注射IL-1后,这些功能就会受损。
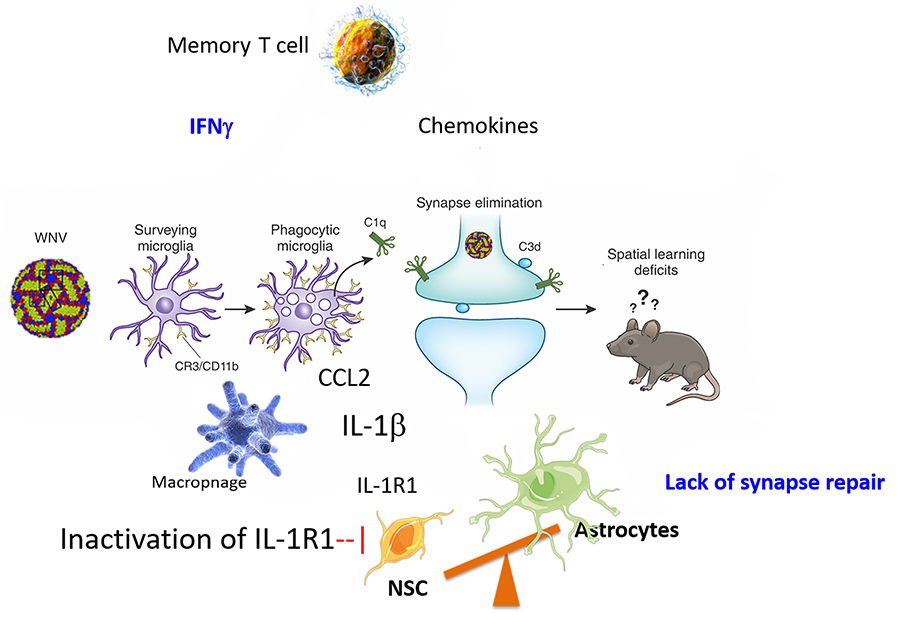
从Klein,R.S.,Garber,C.,&Howard,N.(2017),https://doi.org/10.1038/ni.3656
在WNV感染的情况下,星形胶质细胞释放大量的IL-1,这导致神经发生产生更多的星形胶质细胞,而不是产生学习和记忆所必需的新神经元。抑制IL-1通路可使正常神经发生和抵抗空间学习缺陷。
为了了解更多病毒,
科林教授的研究表明,靶向IFN-γ或IL-1途径,或补体系统的组分可以防止病毒脑炎恢复期间的记忆障碍。
虽然大多数工作都在WNV和ZIKV完成,但其他新兴病毒激活相同的机制并引发类似的神经系统后遗症。该团队已经开始检查SARS-COV-2对脑功能的影响,因为Covid-19已与神经疾病和传染后的精神病和认知障碍有关。鉴于这些机制可能是普遍的认知疾病,并且没有逆转记忆缺陷的治疗,需要了解病毒感染如何导致进步病理遗忘的疾病和逐渐引起痴呆症,以及如何预防那。
个人反应
由于IFN-γ或IL-1的不同作用,您认为是否有可能针对这些途径来防止记忆缺陷而不造成太多的副作用?

