对癌症的个性化免疫疗法进行重新编程免疫系统
我们的免疫系统不仅对我们对抗细菌,病毒和其他病原体的防御至关重要,但它也在预防和抗击癌症方面发挥了乐曲作用。对癌症的免疫反应是复杂的,涉及抗体和具有宽的白细胞类型的广泛曲目,包括淋巴细胞和其他白细胞。
癌症免疫治疗是指任何利用免疫系统对抗癌症的策略,近年来,多项突破使免疫治疗进入了癌症治疗的前沿。与传统化疗相比,免疫疗法有几个优势,包括减少副作用和通过产生持久的免疫反应抑制癌症复发的潜力。
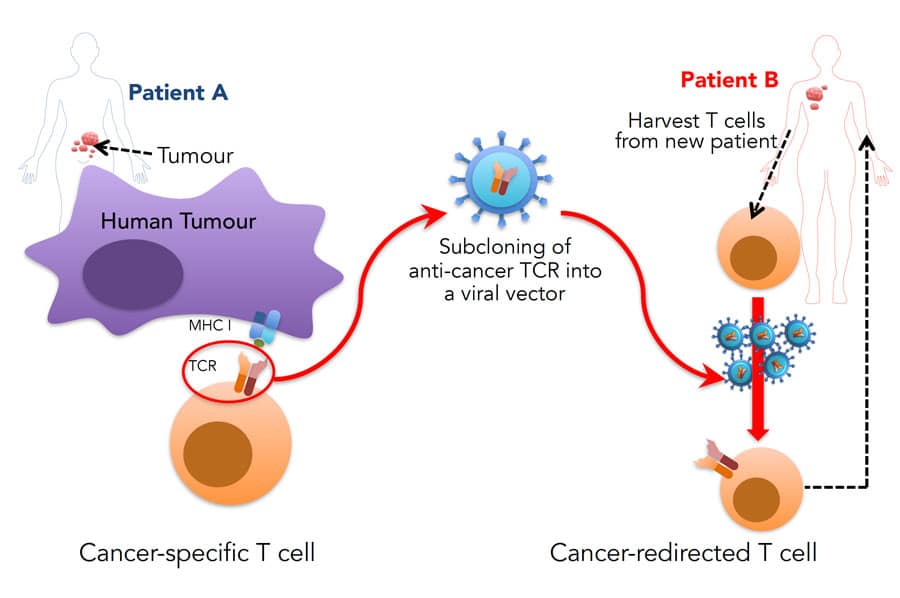
接受癌症信号 - T细胞受体
一类被称为T细胞的白细胞长期以来已知在对癌症的免疫反应中起重要作用。T细胞在其表面上称为T细胞受体(TCR)的信号传导蛋白,该特征将它们与其他白细胞区分开。在复杂的过程中,TCR识别由其他免疫细胞和癌细胞呈递的病原体或肿瘤特异性蛋白质(称为抗原)。
存在几个T细胞子集,每个子集都有自己独特的TCR和专业功能。细胞毒性T细胞和T辅助剂(TH)细胞的特征在于它们的细胞表面上存在CD8或CD4受体。当通过其TCR识别病原体或肿瘤细胞时,细胞毒性T细胞变得活化。随后是释放酶和毒性蛋白质,触发靶细胞中的编程细胞死亡。当他们的名字表明,通过释放称为细胞因子的重要化学信使来帮助其他免疫细胞来帮助其他免疫细胞,从而细化和调节免疫应答。
免疫系统与癌症
癌症免疫学理解的持续进展铺平了新型免疫治疗策略的重大临床翻译方式。癌症疫苗是在20世纪80年代初出现的第一次免疫检查中,具有FDA批准的乙型肝炎病毒(HBV)疫苗,以防止慢性HBV诱导的肝癌。简单来说,使用特异性肿瘤抗原(TA)产生癌症疫苗 - 刺激免疫系统以安装靶向抗肿瘤反应。
虽然癌症疫苗是一种诱人的策略,但癌细胞中存在的免疫抵抗机制可能限制疫苗的长期疗效。尽管在癌症疫苗开发方面作出了巨大努力,但这一领域的进展缓慢。到目前为止,没有一种癌症疫苗被美国食品药品管理局(FDA)和欧洲药品管理局(EMA)批准用于所有个体。
虽然癌症疫苗是一种诱人的策略,但癌细胞中免疫抵抗机制的存在可能限制其长期疗效
采用细胞疗法
虽然开发癌症疫苗的努力继续,但Koya博士在内的研究人员不断探索其他策略。一种这样的策略是基于养护细胞转移(法案)。This is a form of personalised immunotherapy whereby a small number of T cells are taken from a patient’s blood or tumour, sorted and multiplied in vitro (in the laboratory), and then reinfused into the same patient’s blood – in a similar manner to a blood transfusion. ACT usually follows a period of pre-conditioning chemotherapy known as lymphodepletion, where patients’ overall lymphocyte numbers are reduced to maximise the chances of proliferation of the newly infused T cells.
美国国家癌症研究所(National Cancer Institute)在长期观察肿瘤浸润淋巴细胞(TILs)的存在与广泛癌症临床结果的改善有关后,首次证实了ACT的潜力。TILs指的是任何离开血液并迁移到肿瘤中的白细胞。虽然早期的ACT尝试使用体外选择的TILs似乎很有前途,但分离和处理TILs的方法是劳动密集型的,而且只对一部分癌症患者有利。
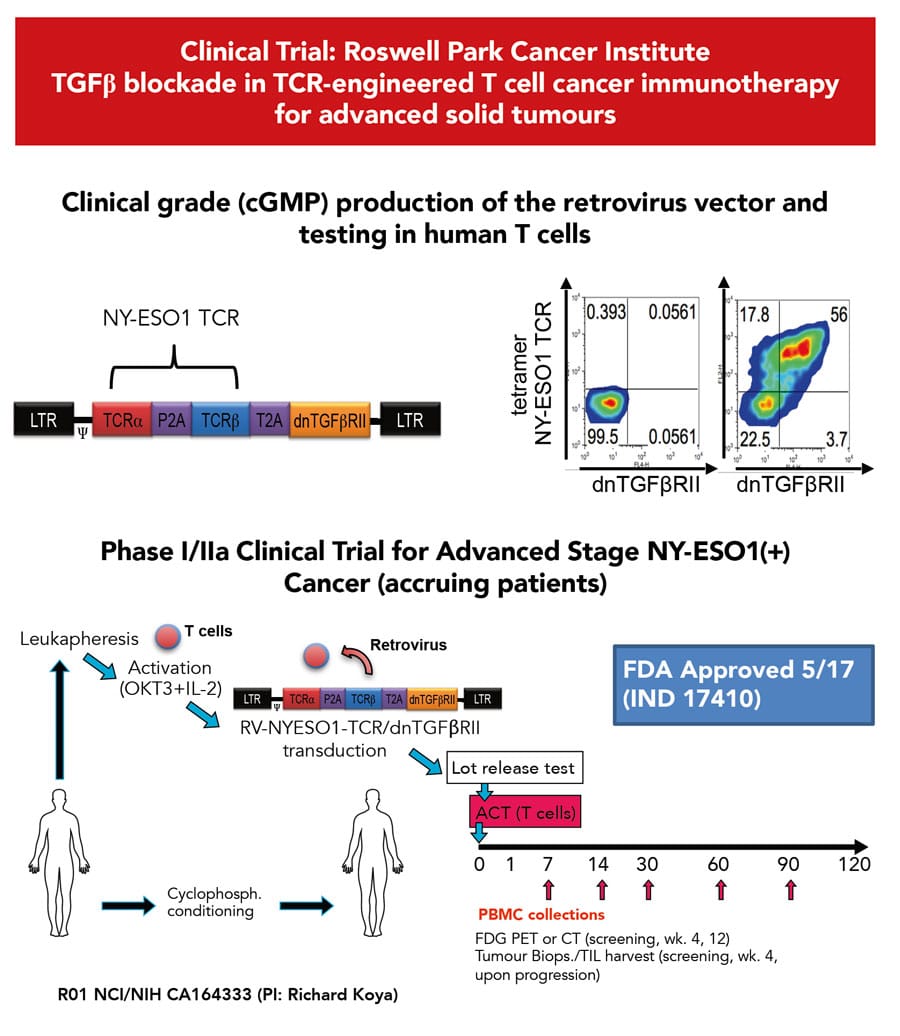
tcr工程T细胞免疫治疗-它在基因中!
十多年来,Koya博士一直致力于推进以青蒿素为基础的高度特异性和持续性癌症治疗。他的研究中心专门针对tcr工程T细胞免疫疗法,利用基因工程重新编程或“再教育T细胞,以极其精确和有效的方式对恶性细胞进行致命打击”。
Koya博士的组利用病毒DNA将TA特异性TCR注入T细胞。然后,这些新插入的受体以高度特异的方式将这些细胞靶向肿瘤。这种方法改善了法案,因为工程化的T细胞在靶向肿瘤中优于靶向肿瘤,而不是早期的ACT尝试中使用的体外直线。换句话说,T细胞专门重新编程以破坏癌细胞。通过在专用实验室条件下扩展这些细胞,可以将数十亿个高活性的肿瘤特异性T细胞注入患者,以高效率和特异性靶向肿瘤。
工程化T细胞作用有可能靶向任何类型的癌症,但迄今为止最广泛研究的癌症是转移性黑色素瘤。
从实验室到诊所
以前的研究根据Koya博士的指导,并且实际上是其他研究群体,揭示了使用转移黑素瘤患者的TCR工程T细胞的作用治疗的显着临床反应。然而,虽然响应率往往超过50%,但大多数患者最终都会看到复发。Koya博士的组假设是高活性TCR工程化T细胞最终屈服于免疫抑制肿瘤微环境 - 一种通过肿瘤细胞分泌转化生长因子β(TGF-β)而大部分施加的环境。Koya博士之前的临床试验经验支持这一假设,目前正在通过Koya博士领导的Roswell Park Cancer Institute在Roswell Park Cancer Institute新的国家卫生资助前瞻性临床试验中进行了测试。
Koya博士的研究利用基因工程对T细胞进行再教育,从而对恶性细胞进行致命打击
该试验专门针对转移性癌症患者的免疫调节剂增强的TCR工程化T细胞转移来具体地解决了一种新的动作方法。该研究采用TCR制造的T细胞转移比TCR - 工程进一步,因为T细胞也被设计成失去对分泌的TGF-β的免疫抑制作用的敏感性。如果假设是正确的,则这些特殊工程化的T细胞应在微管环境中表现出持续疗效,导致较少的复发情况和更好的患者结果。
以前基于ACT的临床试验主要集中在仅使用细胞毒性T细胞。然而,证据正在促进Th细胞在行为中的疗效。自该细胞现在已知促进对癌细胞的细胞毒性T细胞反应的维持,以及借鉴被排出的T细胞,预计可以通过CD8TCR-和CD4TCR工程的T细胞的协同作用来实现持续的免疫应答。在未来的临床试验中可能会调查这种想法。正在调查的另一个大道是与患有癌细胞使用的其他细胞途径抑制免疫系统的疗法的组合。
免疫治疗是一个令人兴奋的领域,新的方法目前正在进行的临床试验中,追求有效的,个性化的癌症治疗。这些疗法可能有一天会成为治疗癌症患者的标准。
问答
您的研究迄今为止最大的技术挑战是什么?
你认为未来免疫治疗的发展有一天会完全取代传统的化疗方法吗?
广泛使用青蒿素联合疗法是否可能产生不良影响或存在安全问题?
有时伴随法案的主要问题是普遍炎症,可以在某些类型癌症患者中发生,副作用称为细胞因子释放综合征。这在基于TCR的疗法中不太常见,但与Car-T细胞的另一种方式更普遍,这种行为的形态更为普遍。
没有一种肿瘤类型对ACT无效;任何固体或液体肿瘤都可以被ACT靶向
您是否预计患者可以在复发后重新提交?
是否有肿瘤类型的行为不太可能有效?


多亏了这本了不起的手册
这真是乐于助人,谢谢。
这是惊人的新闻,迫不及待地想看到它发生了