自适应癌细胞:转移性肿瘤如何进化到抵抗治疗
当一个人死于癌症,原因通常不是原发肿瘤,而是转移瘤。转移是癌细胞离开原发肿瘤并转移到身体其他部位时发生的继发性肿瘤。尽管医学科学最近取得了许多进展,但转移瘤是极其难以治疗的。虽然转移性癌症患者有时可以存活数月或数年,但这种疾病几乎总是致命的,导致全球每年有1000万癌症患者死亡。
需要新的研究途径来应对预防和治疗转移性癌症的挑战。一个新颖的想法是将进化原理应用于癌症。然而,对于许多人来说,“进化”这个词可能会让人联想到更大的物种——例如,人类是从类人猿进化而来的——进化生物学的原则也适用于细胞水平。正常情况下,细胞不仅仅是为了自身利益而运作;每个细胞都有特定的功能,这有助于整个生物体的生存。然而,有时事情会出差错。不需要的基因变化会产生癌细胞,这种癌细胞不受控制地分裂,导致肿瘤的生长。
约翰·霍普金斯大学泌尿学和肿瘤学助理教授萨拉·阿蒙德博士和她的同事们认为,癌症可能经历趋同进化——在这个过程中,相同的特征在不同的物种中出现,这是不同进化过程的结果。例如,鸟类和蝙蝠都有翅膀,但这一特征是不同进化过程的结果。
一种称为多种肺癌细胞(PACC)的一种类型的癌细胞可能代表一系列会聚进化。这些细胞似乎存在于所有转移性疾病患者中的每种类型的癌症中;它们似乎是所有类型癌症的“共同分母”。如果这持有真,那么大多数致命肿瘤都会收敛于杀伤性和抗性的单一表型:研究团队认为是由于PACCS。
前扣带皮层在晚期癌症的发展中起着至关重要和不成比例的重要作用。
癌症会适应不断变化的环境
已经研究了数十年的肿瘤细胞异质性。它描述了癌细胞并不相同的观察。与正常细胞一样,癌细胞对不同的东西擅长,包括它们的生长,分裂和存活的能力。具有再溶解性的癌细胞可以迅速分裂以产生具有许多不同性质的新细胞。通过形成更多多种多变的细胞,有些可能是一些将很好地适应环境,即具有高水平变化的细胞可以进入所需的自适应特征的更大工具箱。对于癌细胞,这意味着从身体自身的化疗的防御中存活所有攻击的能力。这种适应的能力,从而存活变化,以证明对其他细胞的灾难性是一些转移性癌细胞的关键特征。
然而,阿蒙德博士和她的同事们正在引入一个新想法。他们正在将进化的概念——尤其是趋同进化——应用到他们的研究中,研究一些特定的癌细胞如何能够在所有尝试的治疗中存活下来。Amend博士用“进化能力”这个词来描述一些细胞的进化能力;也就是说,发展出可被下一代细胞继承的多种特性的潜力。
博士修正的重点是识别和表征PACC。PACCS显示出一些独特而有趣的性质,有助于发展转移和抵抗治疗。至关重要的是,PACC在几乎所有终癌患者中都存在。这些细胞异常大并且含有远远超过正常遗传物质(DNA)的细胞非常有弹性。这意味着它们不受标准癌症治疗的影响,例如化疗,以及产生PACCS的癌细胞种类更可能出于那些不生存的癌细胞。与其他癌细胞相比,PACC也可能在身体周围移动并侵入其他组织,引发转移性肿瘤的生长。博士认为,这些品质允许采用PACC在终末癌症的发展中发挥批判性和不成比例的作用。
癌细胞存活和茁壮成长
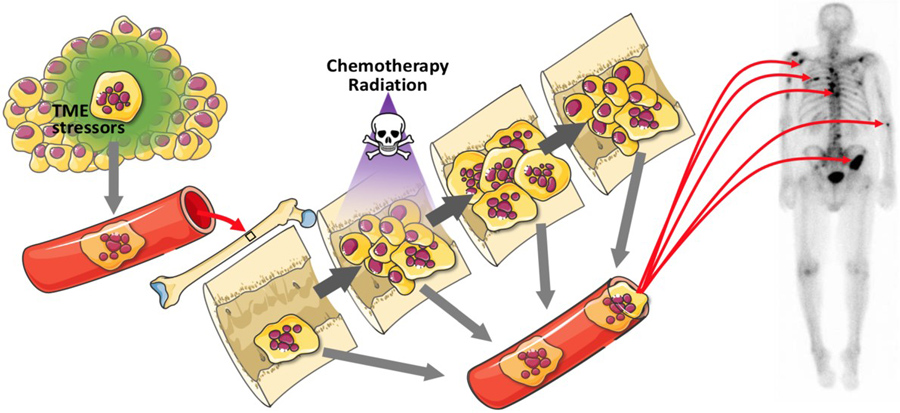
癌症治疗的严谨性可能不仅可以摧毁PACC,它们实际上可能诱导这些阴险细胞的形成。以前的博士修正和同事的研究表明,PACC可以响应压力,包括医疗治疗等化疗。在转移性癌症患者中,PACC在转移中比在原发性肿瘤中更常见。
那么pac是如何在所有试图摧毁它们的行动中幸存下来的呢?答案可能就在他们“装死”的能力中,也就是进入一种被称为“静止”的状态。静止细胞退出细胞周期——细胞生长和分裂的正常过程——但当条件更有利时,仍能重新进入细胞周期。对于pacc来说,这意味着它们可以保护自己的遗传物质,并在暴露于化疗等压力时避免破坏。这一特性也让扣带皮层前部扣带皮层能够在体内游走和入侵其他组织所造成的压力下生存下来。一旦压力被消除——例如,如果化疗被停止——静止的pacc能够重新进入细胞周期,并恢复产生新的癌细胞的过程。
PACC允许癌症在面对意想不到的压力面前持续和生存。进化是遗传变异的作用;可用的变化越多,允许适应环境变化的可能性越高。PACCS的异常大量的遗传物质意味着它们可能包含许多潜在的挑战和胁迫解决方案。变异水平远远大于在正常细胞中发现的水平,例如前列腺或肾细胞。这种遗传变异也允许癌症,通过PACCS加速压力条件的演变。一旦环境更有利,允许进化缓慢。
在pac的案例中,
它们的可进化性可能是它们的衰落。
致死癌的收敛演变
PACC的难以限于人类。PACC的特征也被发现在其他非常不同的物种中,包括细菌等单细胞生物。在这里,它们也响应压力,表明它们可能是古代,祖传遗传编程的结果。与癌症一样,诸如大型和杂乱的遗传物质系列的特征允许单细胞生物快速适应变化的环境。
同样,可以通过其独特的优势来解释各种类型癌症中PACC的外观。PACCS提供遗传变异水平,使癌细胞能够利用广泛的可能解决环境压力和化疗等挑战。
利用PACC治疗癌症
博士修改认为,目标采用PACCS应该是未来癌症治疗的发展的核心。PACCS可能往往负责治疗患者的癌症的重新出现;因此消除癌症要求消除PACC。
一种巧妙的摧毁PACC的方式可能是用自己的优势作为武器。为此,博士修正案建议利用称为“进化陷阱”或“进化双束缚”的现象。在这种情况下,某种物种在对环境变化的反应时出现了某种特征,这意外地使它变得易受不同的威胁。在PACC的情况下,他们的进化可能是他们的垮台。
当一个正常的体细胞分裂时,它的遗传物质,由染色体组织,在两个相似大小的子代细胞中平均分裂。这个过程是由一个叫做中心体的结构控制的,它控制着染色体的相等分裂。对于DNA数量异常的细胞,如pacs,这个过程更加复杂。需要额外的中心体来确保分裂过程不会导致细胞的破坏。一种叫做驱动蛋白14的蛋白质允许额外的中心体正常工作。至关重要的是,虽然pacc依赖于这种蛋白质进行细胞分裂,但正常细胞可以不依赖它而正常工作——这意味着破坏kinesin 14可以消除pacc,而不伤害正常细胞。Amend博士提出,进化陷阱将包括使用化疗通过应激反应来触发pac的产生,然后使用一种专门针对驱动蛋白14的药物。该药物会阻断驱动蛋白14的活性,干扰额外中心体的功能。如果没有驱动蛋白14,pacc将无法分裂和复制自己;如果没有pacc,癌症就很容易受到其他癌症治疗方法的影响。
这些想法还处于早期阶段。在进化陷阱成为转移性癌症患者的可行治疗方法之前,还需要进行更多的研究。然而,阿蒙德博士和她的同事们采用的将进化科学原理应用于癌症的新方法有着巨大的潜力。迄今为止,驱动蛋白14一直是研究的重点,该团队也希望调查其他潜在的目标。无论是通过驱动蛋白14还是其他途径,寻求针对pacc的独特特征,可以提供新的和有效的方法来对抗转移性癌症,为患有这种目前无法治愈的疾病的人们带来希望。
个人反应
除了Kinesin 14,是否有其他潜在的“进化陷阱”,可用于开发新的治疗方法?


患有子宫内膜腺癌,浆液性13年。切除手术切除包括子宫颈在内的所有女性器官我接受了三次完整的化疗,直到最后一次化疗时我对卡铂过敏。几个放射治疗。的目标。转移到两肺。还有肝脏和甲状腺。在临终护理中心,但现在严格的旧石器饮食,以及非常规的药物、维生素和补充剂。我变得更好。这篇文章给了我们一些希望。